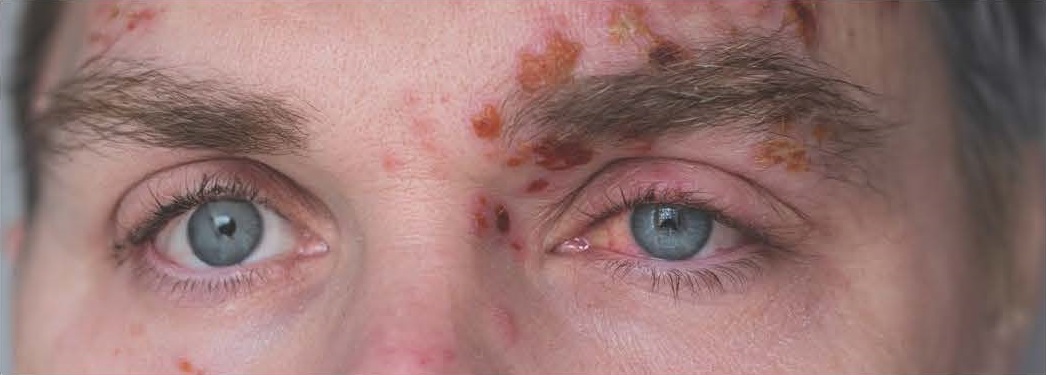
Dne 1. března 2024 byl na našem očním oddělení vyšetřen 55letý pacient s hlavní stížností na zarudnutí levého oka trvající od 26. února. Před zarudnutím levého oka potvrzuje virové onemocnění. Od 29. února se objevil kožní exantém na levé časti obličeje v distribuci první větve trigeminu.
Pacientovi byl diagnostikován herpes zoster ophthalmicus (HZO) a dendritická keratitida levého oka, Hutchinsonův znak byl negativní. Po našem oftalmologickém vyšetření byl pacient odeslán na kožní kliniku k hospitalizaci a byl mu intravenozně podán acyklovir.
Lokální léčba byla zahájena mastí Tobrex (tobramycin – ATB) pětkrát denně a Virgan gelem (gancyklovir) čtyřikrát denně. Pacient byl hospitalizován na kožním oddělení od 1. do 8. března.
Během hospitalizace navštívil naše oddělení několikrát s komplikací, lehkou přední uveitidou na levém oku. Po propuštění z kožního oddělení pokračoval týden v per os Zovirax (acyklovir) 800 mg tbl pětkrát denně.
Celkem navštívil naše oční oddělení šestkrát v průběhu 2 týdnů. Jeho poslední oční vyšetření bylo 15. března, kdy bylo patrné úplné vymizení očního nálezu, nicméně byla patrná hyperpigmentace levé části obličeje v distribuci první větve trigeminu nervu (n. ophthalmicus).
Kvůli přetrvávající postherpetické neuralgii byl odeslán k dalšímu ošetření do ambulance bolesti naší nemocnice.