Effekt
RUBY: Randomisert kontrollert studie av dostarlimab i kombinasjon med karboplatin og paklitaksel til behandling av voksne pasienter med primær fremskreden eller tilbakevendende EC.
Effekten og sikkerheten til dostarlimab i kombinasjon med karboplatin-paklitaksel ble undersøkt i en multisenter, randomisert, dobbeltblindet, placebokontrollert fase 3-studie utført på pasienter med primær fremskreden eller tilbakevendende EC.
De primære effektmålene var progresjonsfri overlevelse (PFS) som vurdert av utprøver i henhold til RECIST v1.1 hos pasienter med dMMR/MSI-H primær fremskreden eller tilbakevendende EC og hos alle pasienter (samlet ITT-populasjon) med primær fremskreden eller tilbakevendende EC, samt total overlevelse (OS) hos alle pasienter (total ITT-populasjon) med primær fremskreden eller tilbakevendende EC.
Totalt 494 pasienter med EC ble vurdert for effekt i RUBY-studien. Demografiske data og karakteristika ved baseline: median alder 65 år (38 % i alderen 65 til 74 år og 13 % i alderen 75 år eller eldre); 77 % hvite, 12 % svarte, 3 % asiatiske; ECOG PS 0 (63 %) eller 1 (37 %); primær stadium III 19 %, primær stadium IV 34 %, tilbakevendende EC 48 %; endometrioid karsinom 55 %, blandet karsinom 4 %, karsinosarkom 9 %, klarcellet karsinom 3 %, serøst karsinom 21 %, annet 8 %; og tidligere kirurgi 91 %, tidligere strålebehandling (28 %), tidligere kreftbehandling (20 %).
Identifiseringen av dMMR/MSI-H-tumorstatus ble prospektivt bestemt basert på lokale testanalyser (IHC, PCR eller NGS), eller sentral testing (IHC) når ingen lokale resultater var tilgjengelige.
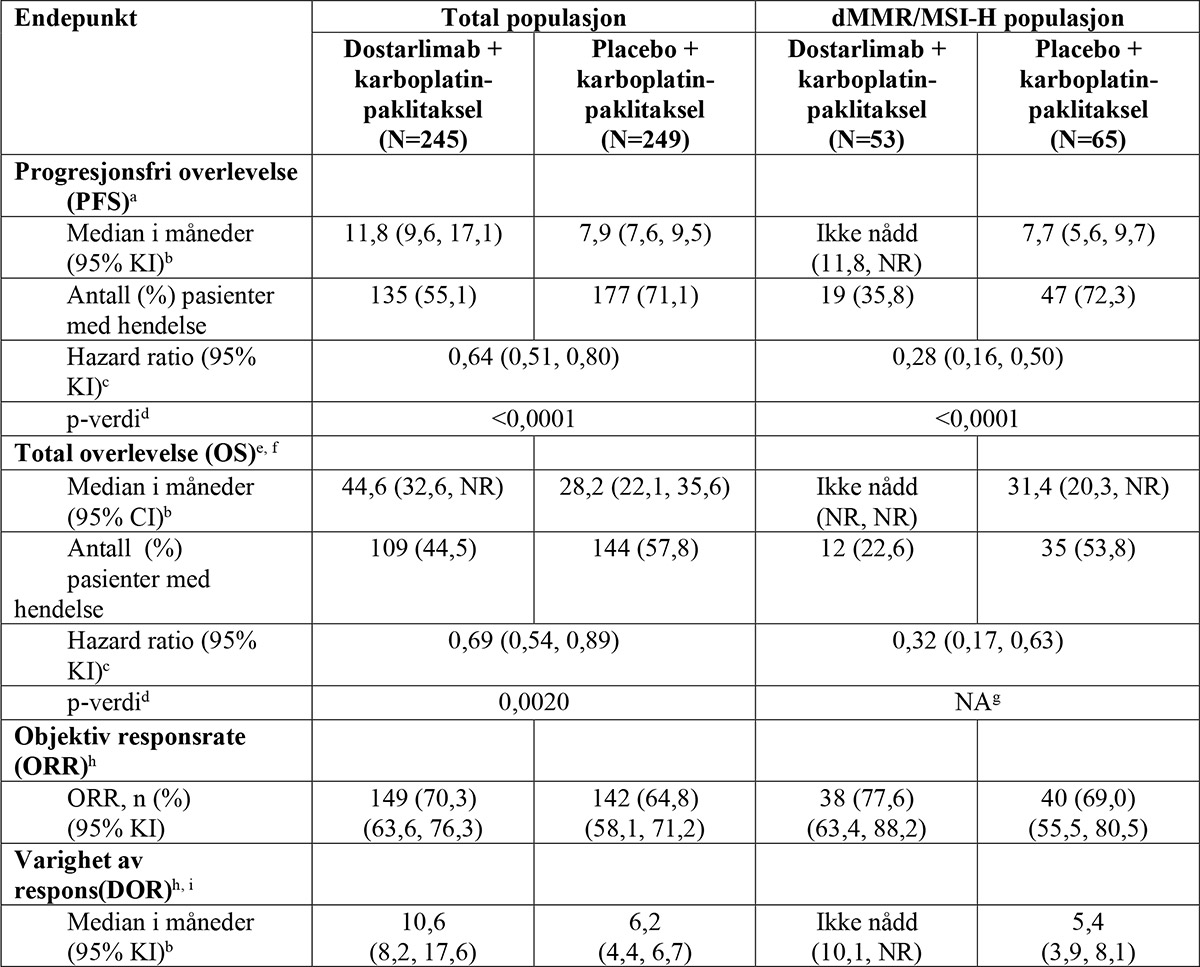
Effektresultater er vist i tabell 5. PFS presenteres ved primæranalysen med median oppfølging på 25 måneder. OS-resultater er basert på den andre interimanalysen med median oppfølging på 37 måneder. Dostarlimab + karboplatin-paklitaksel viste statistisk signifikante forbedringer i PFS av utprøver (dMMR/MSI-H og totale populasjoner) og OS (total populasjon) versus placebo pluss karboplatin-paklitaksel.1