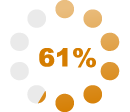
Över en tredjedel av de som svarade på JEMPERLI fick en komplett respons (n = 23/65)
- Mer än hälften av patienterna (60,1 % n = 86/143 sjukdomskontroll) (95% KI: 51,6, 68,2) såg inte sin sjukdom förvärras när de behandlades med JEMPERLI1
Är du inte hälso-eller sjukvårdspersonal? Besök då i stället vår hemsida för allmänheten
Inte hälso- och sjukvårdspersonal? Besök gärna vår allmänna hemsida.

Anoro Ellipta 20 mcg
har lagts i din kundkorg
59
Fokus på förlängd överlevnad1
Godkänt för att användas i kombination med karboplatin och paklitaxel för första linjens behandling av vuxna patienter med primär avancerad eller recidiverande endometriecancer för vilka systemisk behandling är lämplig.1
Primära utfallsmått: ORR och DOR*
Säkerhet i Analysen
605 patienter med EC eller andra solida tumörer
Säkerhet och OS i Analysen
153 patienter med dMMR/MSI-H EC
Effekt i Analysen
143 patienter med dMMR/MSI-H-EC som hade en mätbar sjukdom vid baslinjen och minst 24 veckors uppföljning
Patienterna fick: JEMPERLI 500 mg var 3:e vecka i 4 doser följt av 1 000 mg var 6:e vecka1†
*Enligt bedömning i en blindad oberoende central granskning (BICR) i enlighet med svarsbedömningskriterierna för solida tumörer version 1.1 (RECIST v1.1).1
†Fortsatt behandling fram till sjukdomsprogress eller oacceptabel toxicitet.1
| Utvalda Inklusionskriterier1,2 | Utvalda Exklusionkriterier1,2 |
|---|---|
| Recidiverande eller avancerad endometriecancer |
Tidigare behandling med PD-1/PD-L1 hämmare eller annan immuncheckpointhämmarbehandling. |
| dMMR endometriecancer bestämt genom IHC-testning | Automimmun sjukdom som krävt systemisk behandling inom två år före studien |
| Progression på eller efter platinuminnehållande behandling |
Immunbristsjukdomar, inklusive historik av HIV-infektion, hepatit B eller hepatit C. |
| ≤2 tidigare anti-cancerbehandlingar för rediverande eller avancerad sjukdom |
| Patientpopulation1,2 |
|---|
| Patienter ≥ 18 år |
| Recidiverande eller avancerad endometriecancer som har progredierat under eller efter behandling med en platinuminnehållande behandling |
| dMMR/MSI-H-tumörstatus bestäms prospektivt genom lokal testning |
dMMR = mismatch repair deficient (defekt felmatchningsreparation), EC = endometrial cancer (endometriecancer), HIV = human immunodeficiency virus (humant immunbristvirus), IHC = immunohistochemistry (immunhistokemi), MSI-H = microsatellite instability (mikrosatellitinstabilitet), PD-1 = programmed death receptor 1 (programmerad dödsreceptor 1), PD-L1 = programmed death ligand 1 (programmerad dödsligand 1).

65 år medianålder

63% av patienterna hade genomgått en tidigare behandling
Histologi

64,3%
endometroida
karcinom typ 1

34,3%
endometroida
karcinom typ 2

1,4%
okänd status
ECOG-status

ECOG 0
ECOG 1
FIGO-stadium

56.6%
Stage III or IV
at time of diagnosis
56,6%
Stadium III eller IV
vid tiden för diagnos
ECOG = Easter Cooperative Oncology Group
FIGO = International Federation of Gyneacological Oncology

Över en tredjedel av de som svarade på JEMPERLI fick en komplett respons (n = 23/65)
CI/KI = confidence interval (konfidensintervall), CR = complete response (komplett respons), ORR = objective response rate (objektiv svarsfrekvens), PR = partial response (partiell respons).
Svarsduration

svarade fortfarande vid 12 månader

svarade fortfarande vid 24 månader
Median-DOR nåddes inte (1,2+ till 47,2+) med en medianuppföljning på 27,6 månader.
54 AV 65 SVARANDE FORTSATTE ATT SVARA FRÅN OCH MED CUT-OFF FÖR DATA3
VID RECIDIVERANDE/AVANCERAD DMMR/MSI-H-EC EFTER PLATINABASERAD BEHANDLING
JEMPERLI är avsett att användas i kombination med karboplatin och paklitaxel för första linjens behandling av vuxna patienter med primär avancerad eller recidiverande endometriecancer för vilka systemisk behandling är lämplig.
JEMPERLI är avsett som monoterapi för behandling av vuxna patienter med recidiverande eller avancerad endometriecancer med dMMR (mismatch repair deficient) eller hög mikrosatellitinstabilitet (MSI‑H) som har progredierat under eller efter tidigare platinainnehållande behandling.1
Detta läkemedel är föremål för utökad övervakning.
JEMPERLI (dostarlimab), 10 ml koncentrat till infusionsvätska, lösning, innehåller 500 mg. Rx, EF. ATC-kod: L01FF07, Monoklonala antikroppar och antikroppsläkemedelskonjugat.
Indikationer:
Dosering:
Varningar och försiktighet:
För fullständig förskrivarinformation och pris, se www.fass.se. Tidpunkt för översyn av produktresumén 2026-02-10 GlaxoSmithKline AB, Box 516, 169 29 Solna, telefon: 08-638 93 00, se.gsk.com.
Referenser
Om du vill rapportera en biverkning på något av våra läkemedel eller vacciner så kan du kontakta oss på följande sätt: Webformulär: se.gsk.com/biverkning. Telefon: 08-638 93 00 (be om att bli kopplad till Biverkningsenheten). Brev: GSK AB, Box 516, 169 29 Solna.
PM-SE-DST-WCNT-240005, November 2025




